Cinética de Troca Iônica
1. Introdução
Se procurarmos a definição de cinética na internet nos depararemos com algo do tipo “Cinética (física): o estudo das forças associadas ao movimento, incluindo forças causadoras de movimento e forças resultantes de movimento.” Com base nesta definição, podemos entender que a cinética aplicada ao estudo da troca iônica está interessada em descrever com que velocidade os íons presentes na solução transferem-se para a fase sólida, e vice-versa. Não somente a velocidade, mas também está interessada em entender quais fenômenos influenciam na velocidade da troca iônica e porque são causados.
2. Cinética de Troca Iônica
A Figura 1 apresenta os mecanismos presentes durante a troca iônica de um componente j, inicialmente na fase líquida, o qual se transfere até a fase sólida (resina de troca iônica), de um ponto de vista de uma única esfera isolada.
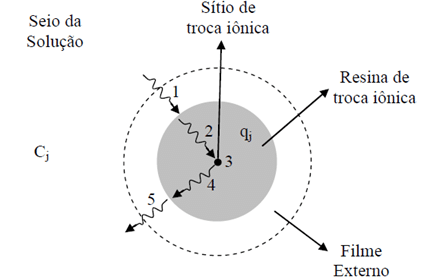
As etapas numeradas na Figura 1 são:
1. Difusão de j no filme líquido que envolve a partícula de resina (difusão no filme externo);
2. Difusão de j no interior dos poros da partícula de resina até o sítio de troca iônica;
3. Reação de troca iônica;
4. Difusão do contra-íon (inicialmente na resina) através dos poros da resina;
5. Difusão do contra-íon no filme líquido externo que envolve a partícula de resina;
A etapa controladora do processo é tida como a etapa mais lenta, e pode ser composta apenas por uma das etapas ou então por uma combinação entre elas. Em geral, para troca iônica a etapa de reação (3) ocorre rapidamente e não impõem resistência ao processo, assim as etapas controladoras da velocidade de troca iônica são as etapas de transferência de massa (1, 2, 4 e 5).
O processo de difusão no sólido ainda pode ser separado em três processos que ocorrem por mecanismos distintos:
I. Difusão nos macroporos;
II. Difusão nos microporos;
III. Difusão em um sólido homogêneo;
Segundo Perry e Green (2008), para resinas de troca iônica do tipo gel, a etapa de transferência de massa no sólido pode ser modelada como difusão em um sólido homogêneo, uma vez que o volume de líquido no interior dos poros da resina tende a zero (poros muito pequenos). Porém o cenário muda com o aumento do tamanho dos poros tornando esta hipótese inválida.
De forma geral, se tivermos interessados em saber os perfis de concentração dos íons na esfera de resina, seja na etapa de operação ou na etapa de regeneração, é necessário a resolução de equações que descrevem as etapas de transferência de massa no processo.
A taxa de transferência de massa da fase líquida para fase sólida é determinada por meio da conservação da massa para fase sólida em conjunto com o mecanismo de transporte apropriado. Desta maneira, é possível prever com que velocidade o íon de interesse j é retido pelo trocador iônico. Esta metodologia é fenomenológica, e pode ser utilizado para prever a transferência de massa entre as fases em sistemas em batelada, leito fixo ou outros equipamentos de contato para troca iônica ou adsorção (PERRY e GREEN, 2008).
Para uma partícula esférica, porosa, por onde transporta-se um íon j, escreve-se o balanço de massa em coordenadas esféricas como:
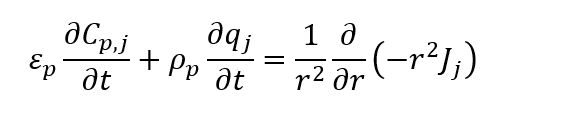
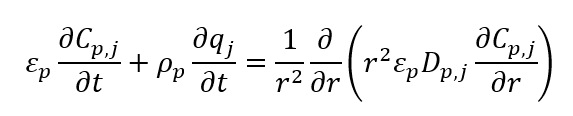
Para resinas do tipo gel, a hipótese de sólido homogêneo reduz a expressão à:
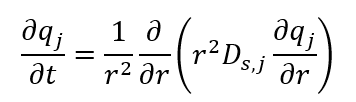
Analisando as expressões acima notamos que sua solução fornecerá o perfil de concentração do íon j ao decorrer do raio r da esfera de resina em um tempo especificado. Os métodos para obter as soluções que revelam o perfil de concentração no interior das esferas de resina não são triviais e hoje a aplicação desta teoria em projetos de troca iônica fica restrita ao âmbito acadêmico e projetos especiais.
Mesmo que a solução destas expressões cinéticas não sejam uma atividade rotineira para as principais aplicações já bem estabelecidas da troca iônica no segmento de tratamento de água, seu entendimento fornece base para a compreensão de como e porque algumas variáveis influênciam no processo, seja na etapa de operação ou regeneração das resinas.
3. Relacionando Teoria e Prática
Para entender a importância dos conceitos descrito a cima, analisaremos situações cotididianas presentes em aplicações simples e bem estabelecidas de resinas de troca iônica ao tratamento de água. Na etapa de regeneração das resinas uma das recomendações sempre encontradas em documentos técnicos de fabricantes é o tempo de contato entre o regenerante e a resina. Para íons inorgânicos o tempo recomendado situa-se em média de 20 até 40 minutos para o contato da solução de químico regenerante com o leito de resina. A Figura 2 apresenta a evolução do grau de regeneração de uma resina catiônica aplicada ao abrandamento de água de acordo com o tempo de contato com salmoura com 10% de concentração.
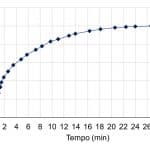
Como esperado, a regeneração é mais eficiente com o aumento do tempo de contato, uma vez que a difusão é mais efetiva. Porém, ao compararmos a Figura 2 com a Figura 3, tem-se uma notável diferença de escala de tempo de contato para alcançar graus elevados de regeneração.
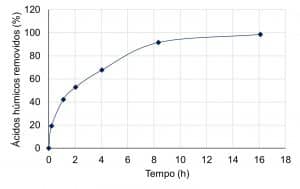
Para expulsar moléculas de ácido húmico do interior da resina necessitamos de um tempo de contato muito maior, quando comparado aos cátions inorgânicos. Isto ocorre devido a menor velocidade de difusão das grandes moléculas nos pequenos poros das resinas de troca iônica. Desta forma, para obter eficiências de regeneração aceitáveis para moléculas orgânicas, necessitamos aumentar o tempo de contato.
Outra alternativa para aumentar a a eficiência de regeneração e acelerar a velocidade de difusão seria manipular variáveis do processo de forma a contribuir para o aumento do coeficiente de difusão da espécie na estrutura da resina. Para o caso de remoção de orgânicos da água, duas estratégias seriam a alteração da concentração dos regenerantes (ação limitada por características de resistência física das resinas) ou então aumentar a temperatura da solução regenerante, variável que afeta diretamente a velocidade de difusão das espécies (porém, também limitada por motivos de resistência da matriz polimérica).
A Figura 4 apresenta como a concentração de NaCl afeta a eficiência de regeneração de resinas catiônicas aplicadas ao abrandamento de água. No eixo das ordenadas temos o fator de correção de capacidade de troca iônica o qual é obtido ao fixarmos o valor da concentração de NaCl no eixo das abscissas. Fatores de correção menores que 1 indicam perda de eficiência de regeneração para a concentração de NaCl adotada.
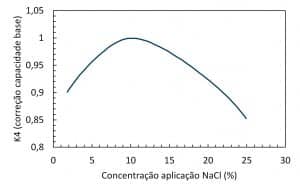
Nota-se que o fator aumenta até 1 ao atingirmos a concentração de 10% NaCl (não é por concidência que as recomendações de projeto recomendam 10% para regeneração de abrandadores). A medida que a concentração de NaCl aumenta, aumentamos também a força motriz para a transferência de massa, ou seja, aceleramos a difusão dos cátions de sódio na matriz da resina e com isso aceleramos também a expulsão da dureza retida na resina durante a operação. Ao fazemos isso estamos manipulando as condições cinéticas envolvidas no processo. A perda de eficiência acima de 10% não está relacionada a propriedades cinéticas. Era de se esperar melhoria no processo de regeneração aumentando ainda mais a concentração, devido ao aumento ainda maior na força motriz de difusão. Contudo, esta perda de eficiência está relacionada a características de resistência e degradação das resinas devido as propriedades de expansão e contração da matriz polimérica, as quais são influenciadas por propriedades osmóticas.
4. Conclusão
Até aqui não fizemos nenhum cálculo avançado com as equações cinéticas apresentadas, porém, relacionamos comportamentos fundamentais do processo de troca iônica com a teoria fundamental de funcionamento do processo. Desta forma explicamos algumas recomendações e o porque elas seguem esta tendência. O conhecimento de algumas propriedades fundamentais apresenta utilidade prática quando precisamos otimizar processos e buscar melhorias operacionais.
Autor: Mauro Júnior
LEIA TAMBÉM: CONCEITO DE SMART WATER MUDA SETOR DE SANEAMENTO BÁSICO
LEIA TAMBÉM: FUNDO HOLANDÊS DE 7,5 BI DE EUROS PODE FAVORECER HUB DE HIDROGÊNIO VERDE DO PECÉM
























